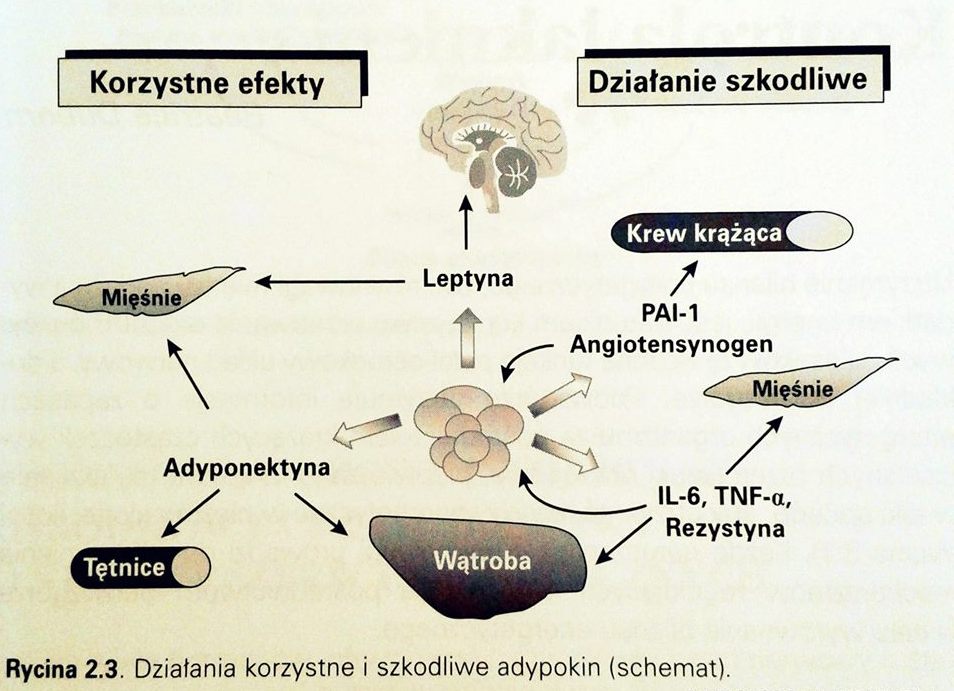
Cechy szczególne wydzielniczej czynności tkanki tłuszczowej.
Długo uznawano tkankę tłuszczową jedynie za miejsce magazynowania tłuszczów i dopiero odkrycie leptyny w 1994 roku przyczyniło się do odkrycia jej czynności wydzielniczej. Coraz większe znaczenie patofizjologiczne nadawane tej “nowej” czynności jest związane z jednej strony z licznymi i rozmaitymi działaniami wydzielanych czynników, a z drugiej – ze szkodliwymi skutkami zaburzeń tej czynności w związku z wahaniami masy ciała. Jednak szczególne cechy tkanki tłuszczowej sprawiają, że jest ona nietypowym narządem wydzielniczym. Po pierwsze, jest ona rozproszona w organizmie, tworząc oddzielone od siebie skupiska różniące się wydzielanymi substancjami w zależności od lokalizacji. Po drugie, substancje wydzielane przez tkankę tłuszczową są produkowane przez różne komórki. Niektóre czynniki są produktem samych adypocytów, a inne są wytwarzane przez komórki podścieliska, w tym makrofagi, które u ludzi otyłych przenikają do tkanki tłuszczowej i są ważnym źródłem cytokin. Wreszcie tkanka tłuszczowa wytwarza substancje, które nie są dla niej swoiste, ale są również produkowane przez inne narządy, np. wątrobę.
Czynniki wydzielane przez tkankę tłuszczową oraz przemiana węglowodanów i tłuszczów
Przerost tkanki tłuszczowej związany jest z opornością obwodową na insulinę. Uwalniane w dużych ilościach u osób otyłych kwasy tłuszczowe hamują przemianę glukozy w cyklu Randle`a.
Początkowo badania skupiały się na czynniku martwicy nowotworu (tumor necrosis factor α( (TNF-α), cytokinie prozapalnej, która hamuje pierwsze etapy regulacji insulinowej. Neutralizacja TNF- α poprawia wrażliwość na insulinę. TNF- α pełni funkcję parakrynną w tkance tłuszczowej, powodując miejscową insulinooporność adypocytów i wpływając na wydzielanie innych adypokin.
Interleukina 6 (IL-6) jest wydzielana w dużych ilościach przez tkankę tłuszczową. Przyjmuje się, że jeśli nie toczy się ostry proces zapalny, 10-30% IL-6 zawartej w osoczu pochodzi z tkanki tłuszczowej. Wiele badań ustaliło ponad wszelką wątpliwość istnienie zależności między stężeniem osoczowym IL-6 i BMI z jednej strony, a insulinoopornością z drugiej. IL-6 powoduje insulinooporność w wątrobie, w mięśniach i w tkance tłuszczowej, hamując fosforylację receptora insulinowego.
Również inne substancje produkowane przez tkankę tłuszczową wpływają na regulację gospodarki insulinowej. Należy do nich rezystyna. Stężenie rezystyny jest podwyższone w osoczu otyłych myszy, u których podawanie przeciwciał przeciw rezystynie poprawia wrażliwość n insulinę. Podwyższenie stężenia rezystyny przez podawanie białka lub przez zwiększenie ekspresji genu rezystyny u myszy powoduje obwodową insulinooporność i zwiększenie produkcji glukozy przez wątrobę. U myszy wychudzonych występuje odwrotny fenotyp. Rola rezystyny u człowieka pozostaje wciąż niejasna, zważywszy na sprzeczne doniesienia dotyczące jej stężenia w surowicy ludzi otyłych.
Dwie cytokiny: leptyna i adyponektyna, wywierają korzystny wpływ na gospodarkę węglowodanową. Szczegóły działania leptyny omówię w innym poście. W tym miejscu należy wspomnieć, że w modelu zwierzęcym na skutek niedoboru leptyny rozwija się ciężka insulinooporność. Można ją częściowo odwrócić za pośrednictwem leptyny i mechanizmu aktywującego kinazę AMP w mięśniach szkieletowych. AMPK rozpoczyna reakcję utleniania kwasów tłuszczowych w mitochondriach, umożliwiając rozproszenie lipidów mięśniowych, których obecność w nietypowym miejscu niweluje działanie insuliny. Zmniejszenie działania leptyny (leptynooporność) u osób otyłych ogranicza korzystny wpływ tego hormonu na gromadzenie się lipidów w tkankach innych niż tłuszczowa i jest jednym z czynników wywołujących insulinooporność.
Adyponektyna różni się od innych adypokin tym,że jej stężenie maleje, a nie rośnie u osób otyłych. Ta szczególna właściwość jest spowodowana, przynajmniej częściowo, hamowaniem produkcji adyponektyny przez TNF- α i IL-6. Stężenie adyponektyny wzrasta w odpowiedzi na zmniejszenie masy ciała i w reakcji na poprawę wrażliwości na insulinę. Fakt ten pozwala podejrzewać, że niedostateczne wytwarzanie adyponektyny zaburza równowagę gospodarki węglowodanowej u osób otyłych. Adyponektyna, podobnie jak leptyna, aktywuje AMPK w mięśniach i nasila działanie pobudzające insuliny na obwodową przemianę glukozy. Co więcej adyponektyna wywiera działanie na wątrobę, gdzie za pośrednictwem AMPK hamuje glukoneogenezę i wytwarzanie glukozy. Oprócz korzystnego działania na gospodarkę węglowodanową adyponektyna wywiera również działanie przeciwmiażdżycowe. Wiele badań in vitro wykazało, że utrudnia ona przylegnie monocytów do komórek śródbłonka, hamuje powstawanie komórek piankowatych i przemieszczanie się oraz proliferację mięśniówki gładkiej aorty.
Substancje czynne wydzielane przez tkankę tłuszczową i patologia naczyń krwionośnych
Powikłania naczyniowe u osób otyłych mają kilka przyczyn, a wśród nich niedobór czynnika fibrynolizy, co zwiększa ryzyko zakrzepów. Hamowanie fibrynolizy jest spowodowane w głównej mierze przez zwiększenie stężenia krążącego PAI-1, inhibitora tkankowej aktywacji plazminogenu. PAI-1 jest glikoproteiną wytwarzaną przez wiele typów komórek, między innymi adypocyty. Wiele badań udowodniło istnienie u człowieka zależności między stężeniem krążącego PAI-1 i stopniem otyłości. U człowieka ekspresja mRNA dla PAI-1 w tkance tłuszczowej jest bez wątpienia zwiększona, zwłaszcza w tkance tłuszczowej brzucha. Jednak badania przeprowadzone in vivo nie udowodniły tak jak się stało w przypadku TNF- α, że tkanka tłuszczowa wydziela PAI-1. Wynika z tego, że nawet jeśli istnieje związek między otyłością, tkanką tłuszczową i PAI-1, zwiększenie wydzielania tej ostatniej substancji przez tkankę tłuszczową nie jest wystarczające do zwiększenia jej stężenia osoczowego u osób otyłych.
Tkanka tłuszczowa zwłaszcza głęboka, jest ważnym źródłem pozawątrobowego angiotensynogenu. Liczne badania wykazują dodatnią zależność między wytwarzaniem angiotensynogenu w tkance tłuszczowej i BMI. Angiotensynogen jest prekursorem angiotensyny II w układzie renina-angiotensyna. Angiotensyna II bierze udział w regulacji ciśnienia tętniczego krwi na poziomie nadnerczy, nerek, i mięśni gładkich naczyń krwionośnych oraz w ośrodkowym układzie nerwowym. Wydzielanie angiotensynogenu przez komórki tłuszczowe ma znaczenie zarazem miejscowe i ogólne. U myszy pozbawionych angiotensynogenu można zaobserwować niedorozwój tkanki tłuszczowej, ponieważ angiotensyna II aktywuje wczesne etapy adypogenezy. Myszy te wykazują również niedociśnienie tętnicze. Ponowne wprowadzenie genu dla angiotensynogenu do tkanki tłuszczowej powoduje znaczący przyrost masy tłuszczowej i zwiększenie wartości ciśnienia tętniczego krwi. U dzikich (nietransgenicznych)myszy nadmierna ekspresja angiotensynogenu w tkance tłuszczowej powoduje zwiększenie masy tłuszczowej i nadciśnienie tętnicze. Wynika z tego, że nadmierna produkcja angiotensynogenu przez tkankę tłuszczową może zarówno pobudzić jej rozrost, jak i powodować nadciśnienie tętnicze u osób otyłych.
Podsumowując tkanka tłuszczowa, główne ogniwo homeostazy energetycznej spełnia dwie funkcje. Z jednej strony gromadzi i w razie potrzeby uwalnia zgromadzone zapasy dzięki wyspecjalizowanym komórkom – adypocytom, a z drugiej uwalnia cząsteczki biologicznie czynne, adypokiny, które biorą udział w kontroli tworzenia tkanki tłuszczowej (adypogenezy), w metabolizmie węglowodanów i tłuszczów oraz w regulacji odżywiania.
Na podstawie:
Lafontan M.: Fat cells:afferent and efferent messages define new approaches to treat obesity. Annu. Rev. Pharmacol. Toxicol.,2005, 45, 119-146.
Mac Dougald O. A., Mandrup S.: Adipogenesis: forces that tip the scales. Trends Endocrinol. Metab., 2002, 13,5-11.
Tounian P.: Rozwój i czynność wewnątrzwydzielnicza tkanki tłuszczowej: Otyłość u dzieci, Wydawnictwo Lekarskie PZWL, 2006, 22-29.


